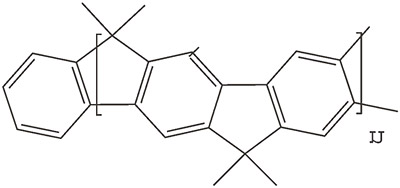
Onderzoekers van de Stichting FOM en de Technische Universiteit Delft hebben ontdekt dat bepaalde typen polymeren uitstekend lading kunnen geleiden. Tot op heden waren alleen polymeren bekend met een geleiding die ruwweg een factor duizend lager lag dan die van conventionele halfgeleiders. De bestudeerde polymeren hebben een soort van ladder structuur en hebben een geleiding die dicht in de buurt komt van conventionele halfgeleiders. Dit is mogelijk doordat deze polymeren een stevige starre 'wervelkolom' hebben waarlangs de lading gemakkelijk kan bewegen. De ontdekking van polymeren met een goede geleiding is een belangrijke stap richting plastic elektronica. Een andere toepassing van de polymeren kan wellicht gevonden worden bij elektronica op moleculaire schaal.

/i/1254411102.png?f=fpa)